Дмитрий Петров (Воронеж)
Мягкая вода и жёсткая вода
 Жесткость воды – это совокупность ее свойств, обусловленных присутствием в ней катионов кальция (Ca2+), магния (Mg2+), и отчасти двухвалентного железа (Fe2+). Различают постоянную, временную и общую жесткость.
Жесткость воды – это совокупность ее свойств, обусловленных присутствием в ней катионов кальция (Ca2+), магния (Mg2+), и отчасти двухвалентного железа (Fe2+). Различают постоянную, временную и общую жесткость.
Общая жесткость определяется суммарным содержанием в воде всех указанных выше катионов.
Постоянная жесткость характеризует количество растворенных сульфатов, хлоридов и некоторых других солей кальция и магния, когда в воде наряду с катионами Ca2+ и Mg2+ имеются анионы SO42-, Cl– и др. При кипячении такой воды концентрации этих катионов и анионов практически не изменяются – отсюда и название «постоянная жесткость».
Временная жесткость связана с присутствием в воде наряду с катионами Ca2+, Mg2+ и Fe2+ гидрокарбонатных или бикарбонатных анионов (HCO3-). При кипячении воды гидрокарбонаты разлагаются, образуя очень плохо растворимый карбонат кальция, углекислый газ и воду: Ca2+ + 2HCO3- = CaCO3↓ + H2O + CO2↑
Если в воде содержится сколько-нибудь значимое количество ионов железа (Fe2+ ) то осадок приобретает жёлтый или даже рыжий цвет по причине образования FeCO3 , а затем в присутствии растворённого в воде кислорода Fe(OH)3, чем больше в воде железа тем сильнее окрашена накипь.
Вода с большим содержанием таких солей называется жёсткой, с малым содержанием — мягкой. Термин «жёсткая» по отношению к воде исторически сложился из-за свойств тканей после их стирки с использованием мыла на основе жирных кислот — ткань, постиранная в жёсткой воде, более жёсткая на ощупь. Жёсткая вода при умывании сушит кожу, в ней плохо образуется пена при использовании мыла. Использование жёсткой воды вызывает появление осадка (накипи) на стенках котлов, в трубах и т. п. В то же время, использование слишком мягкой воды может приводить к коррозии труб, так как в этом случае отсутствует кислотно-щелочная буферность, которую обеспечивает гидрокарбонатная (временная) жёсткость. Потребление жёсткой или мягкой воды обычно не является опасным для здоровья, есть данные о том, что высокая жёсткость способствует образованию мочевых камней, а низкая — незначительно увеличивает риск сердечно-сосудистых заболеваний. Вкус природной питьевой воды, например, воды родников, обусловлен именно присутствием солей жёсткости.
Жёсткость природных вод может варьироваться в довольно широких пределах и в течение года непостоянна. Увеличивается жёсткость из-за испарения воды, уменьшается в сезон дождей, а также в период таяния снега и льда.
Минерализованная вода
 В отличие от понятия «жёсткость» минерализация отражает присутствие в воде всех солей и «солей жёсткости» и солей, не оказывающих на жёсткость никакого влияния. Например, растворение в воде любого количества хлорида натрия (поваренной соли) никак не скажется на жёсткости воды, однако повысит её минерализацию.
В отличие от понятия «жёсткость» минерализация отражает присутствие в воде всех солей и «солей жёсткости» и солей, не оказывающих на жёсткость никакого влияния. Например, растворение в воде любого количества хлорида натрия (поваренной соли) никак не скажется на жёсткости воды, однако повысит её минерализацию.
Пресная вода
Вода, содержащая менее 0,5 промилле солей называется пресной (в потребительском понимании). Ледяные массивы в полярных регионах и ледники содержат в себе наибольшую часть пресной воды земли. Помимо этого, пресная вода существует в реках, ручьях, пресных озёрах, а также в облаках. По разным подсчётам доля пресной воды в общем количестве воды на Земле составляет 2,5—3 %.Около 85—90 % запасов пресной воды содержится в виде льда.
|
Солёность в промилле
|
|
Пресная вода
|
Солоноватая вода
|
Минерализованная вода
|
Рапа
|
|
< 0,5
|
0,5—30
|
30—50
|
> 50
|
Распределение пресной воды по земному шару крайне неравномерно. В Европе и Азии, где проживает 70 % населения мира, сосредоточено лишь 39 % речных вод. Первое место в мире по ресурсам пресных вод занимает Россия, только в озере Байкал сосредоточено около 20 % мировых запасов озёрной пресной воды и более 80 % запасов России. При общем объёме 23,6 тыс. км³ в Байкале ежегодно воспроизводится около 60 км³ редкой по чистоте природной воды.
Морская вода
Морская вода — вода морей и океанов. В среднем солёность Мирового океана составляет около 34,72‰, с колебаниями от 34 до 36 ‰. Это значит, что в каждом литре морской воды растворено 35 граммов солей (в основном это хлорид натрия). Морская вода слабо-щелочная, pH варьирует в пределах от 7,5 до 8,4. Относительно высокая стабильность pH связана с наличием карбонатной буферной системы, функционирование которой поддерживается углекислым газом атмосферы. В некоторых местах, где ощущается дефицит пресной воды, например в Гонконге, морскую воду используют в канализационных системах (сливная вода унитазов и др.). Из-за высокой осмолярности морская вода непригодна для полива большинства растений и в аграрном назначении не используется.
Дождевая вода
 Её состав сильно зависит от местности, климата, состояния атмосферы, экологической обстановки и других факторов. Обычно дождевая вода является мягкой, пресной водой pH около 5,6. Кислотность свежесобранной дождевой воды всегда ниже из-за растворённого в ней углекислого газа, но при хранении CO2 улетучивается и pH повышается до значаний, близким к нейтральным. В районах промышленных предприятий, которые выбрасывают оксиды серы и азота, дающие различные кислоты, в том числе и сильные азотную и серную кислоты выпадают кислотные дожди. При кислотности воды рН 5,5 погибают полезные донные бактерии водоёмов, а при рН 4,5 погибает вся рыба, большинство земноводных и насекомых. Кислотные дожди являются большой экологической проблемой.
Её состав сильно зависит от местности, климата, состояния атмосферы, экологической обстановки и других факторов. Обычно дождевая вода является мягкой, пресной водой pH около 5,6. Кислотность свежесобранной дождевой воды всегда ниже из-за растворённого в ней углекислого газа, но при хранении CO2 улетучивается и pH повышается до значаний, близким к нейтральным. В районах промышленных предприятий, которые выбрасывают оксиды серы и азота, дающие различные кислоты, в том числе и сильные азотную и серную кислоты выпадают кислотные дожди. При кислотности воды рН 5,5 погибают полезные донные бактерии водоёмов, а при рН 4,5 погибает вся рыба, большинство земноводных и насекомых. Кислотные дожди являются большой экологической проблемой.
Подземные воды
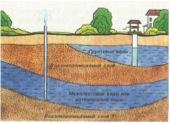 Подземные воды — воды, находящиеся в толще горных пород верхней части земной коры, подразделяются на грунтовые и артезианские.
Подземные воды — воды, находящиеся в толще горных пород верхней части земной коры, подразделяются на грунтовые и артезианские.
Грунтовые воды образуют водоносный горизонт на первом от поверхности водоупорном слое. В связи с неглубоким залеганием от поверхности уровень грунтовых вод испытывает значительные колебания по сезонам года: он то повышается после выпадения осадков или таяния снега, то понижается в засушливое время. В суровые зимы грунтовые воды могут промерзать. Эти воды в большей мере подвержены загрязнению. Грунтовая вода заключена в рыхлых и в слабосцементированных породах (вода пластового типа) или заполняет трещины в каких-либо хорошо сцементированных породах (вода трещинного типа). Она может находиться и в порах пород (поровые воды). Грунтовые воды формируются в основном за счёт инфильтрации атмосферных осадков и поверхностных вод. Область питания грунтовых вод обычно совпадает с областью распространения водоносного горизонта. Мощность горизонта непостоянна и зависит от свойств водосодержащих пород, расстояния до области разгрузки, интенсивности питания и т. д. Главная характерная особенность грунтовых вод, отличающая их от более глубоких артезианских вод — отсутствие напора.
Артезианские воды (от Artesium, латинского названия французской провинции Артуа, где эти воды использовались с XII века) — напорные подземные воды, заключенные в водоносных пластах горных пород между водоупорными слоями. Обычно встречаются в пределах определенных геологических структур (впадин, мульд, флексур и др.), образуя артезианские бассейны. При вскрытии буровой скважиной или шурфом артезианские воды поднимаются выше кровли водоносного пласта, иногда фонтанируют. Источники артезианского типа относятся к важнейшим полезным ископаемым. Обычно залегают на глубине от 100 до 1000 метров.
Питьевая вода, Водопроводная вода («Вода из-под крана»)
 Питьевая вода — это вода, которая предназначена для ежедневного неограниченного и безопасного потребления человеком и другими живыми существами. Главным отличием от столовых и минеральных вод является пониженное содержание солей (сухого остатка), а также наличие действующих стандартов на общий состав и свойства (СанПиН 2.1.4.1074-01 — для централизованных систем водоснабжения и СанПиН 2.1.4.1116-02 — для вод расфасованных в емкости). Общее число микроорганизмов в 1 мл питьевой воды должно быть не выше 100, число бактерий группы кишечных палочек (коли-индекс) – не более 3. Общая жесткость питьевой воды должна быть не выше 7,0 ммоль/л, сухой остаток – 1000 мг/л, рН – от 6,0 до 9,0. Для питьевой В., подаваемой без спец. обработки, по согласованию с органами санитарно-эпидемиологич. службы допускаются след. показатели: сухой остаток – до 1500 мг/л, общая жесткость – до 10 ммоль/л, содержание железа и марганца – соотв. до 1 и до 0,5 мг/л.
Питьевая вода — это вода, которая предназначена для ежедневного неограниченного и безопасного потребления человеком и другими живыми существами. Главным отличием от столовых и минеральных вод является пониженное содержание солей (сухого остатка), а также наличие действующих стандартов на общий состав и свойства (СанПиН 2.1.4.1074-01 — для централизованных систем водоснабжения и СанПиН 2.1.4.1116-02 — для вод расфасованных в емкости). Общее число микроорганизмов в 1 мл питьевой воды должно быть не выше 100, число бактерий группы кишечных палочек (коли-индекс) – не более 3. Общая жесткость питьевой воды должна быть не выше 7,0 ммоль/л, сухой остаток – 1000 мг/л, рН – от 6,0 до 9,0. Для питьевой В., подаваемой без спец. обработки, по согласованию с органами санитарно-эпидемиологич. службы допускаются след. показатели: сухой остаток – до 1500 мг/л, общая жесткость – до 10 ммоль/л, содержание железа и марганца – соотв. до 1 и до 0,5 мг/л.
Дистиллированная и деионизированная вода
 Дистиллированная вода — очищенная вода, практически не содержащая примесей и посторонних включений. Получают перегонкой в специальных аппаратах — дистилляторах.Удельная электропроводность дистиллированной воды, как правило, менее 5 мкСм/см. При необходимости использования более чистой воды используют деионизированную воду. Удельная электропроводность деионизованной воды может быть менее 0,05 мкСм/см. pH=5,4- 6,6. Будучи очень чистой, в отсутствие посторонних механических включений может быть перегрета выше точки кипения, или переохлаждена ниже точки замерзания без осуществления фазового перехода. Фазовый переход интенсивно происходит при введении механических примесей или встряхивании.
Дистиллированная вода — очищенная вода, практически не содержащая примесей и посторонних включений. Получают перегонкой в специальных аппаратах — дистилляторах.Удельная электропроводность дистиллированной воды, как правило, менее 5 мкСм/см. При необходимости использования более чистой воды используют деионизированную воду. Удельная электропроводность деионизованной воды может быть менее 0,05 мкСм/см. pH=5,4- 6,6. Будучи очень чистой, в отсутствие посторонних механических включений может быть перегрета выше точки кипения, или переохлаждена ниже точки замерзания без осуществления фазового перехода. Фазовый переход интенсивно происходит при введении механических примесей или встряхивании.
Бидистиллированная вода — дважды очищенная вода. Близка к химически чистой воде, её получают перегонкой дистиллированной воды в кварцевом аппарате — бидистилляторе или путем обратного осмоса. Для дальнейшей очистки (от летучих органических примесей) бидистиллят облучают гамма-излучением. После облучения для удаления продуктов радиолиза воду продувают очищенным аргоном.
Деионизованная вода — вода, в которой не содержится ионов примесей. Это, фактически, очень хорошо очищенная вода. Её удельное сопротивление составляет 18 МОм·см. Чистота — 99,99999 %. Деионизацию осуществляют с помощью ионообменных смол. Используют смолы двух типов: катионитные R-H (R-органический радикал) и анионитные R-OH. Ионы металлов связываются на катионите. Отрицательные ионы кислотных остатков осаждаются на анионите. Образовавшиеся ионы H и OH объединяются в молекулу воды. Возможно предварительное использование процесса обратного осмоса.
«ЖИВАЯ» и «МЁРТВАЯ» вода
Электроны в молекуле воды сильнее связаны с кислородом, чем с водородом. Поэтому вода способна диссоциировать : H2O <> H+ + OH–
Однако свободный протон не может существовать самостоятельно и гидратируется другой молекулой воды с образованием иона гидроксония : H+ + H2O <> H3O+
Обычно ион H+ переходит от одной молекулы к другой, создавая гидроксильный ион и ион гидроксония, поэтому суммарная реакция запишется как H2O + H2O <> OH– + H3O+
Воздействие на воду постоянным электрическим током с помощью опущенных в неё двух электродов значительно усиливает ионизацию воды и приводит к созданию у электродов более высоких концентраций различных ионов. Это означает, что свойства воды у анода и катода будут различными – происходит ионизация воды. В обычной воде, как известно, присутствуют минералы, поэтому пpи электрическом воздействии происходят более сложные электрохимические реакции. В результате этих реакций у электродов происходит электрохимический синтез новых веществ, отсутствовавших в воде до воздействия тока, однако с прекращением действия тока эти вещества почти мгновенно прекращают своё существование.
Если же воду физически pазделить во вpемя электpовоздействия то пpодукты электрохимической pеакции, находившиеся у pазличных электpодов окажутся в pазных сосудах, и окажутся более стойкими – их пpодолжительность жизни дольше. Это свойство воды называется электpохимической активацией и используется в pазличных областях – в медицине, биологии, металлуpгии и дp. Электровоздействие проводят постоянным током 0,25 – 0,5 A.
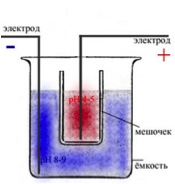 Простейшая установка для электрохимической активации представляет собой сосуд, открытый свеpху, в который помещается "мешочек" из брезента. Один электрод находится внутри этого мешочка, другой вне мешочка. Мешочек изымается до прекращения действия тока. Как вариант возможна конструкция с двумя такими мешочками (для каждого электрода). Образуются продукты электрохимических реакций – анолит и католит, происходят стpуктуpно-энеpгетические изменения воды и ионо-гидpатных образований, изменяется поверхностное натяжение. Анолит образуется в анодной камере. Католит – в катодной содержит гидроокислы и небольшое количество перекиси водорода. Пpи изготовлении электpоактиватоpов используют химически стойкие материалы. В идеальном варианте для изготовления катодов – титан, анодов – платина или графит. Возможно применение нержавеющих сталей, но не все маpки сталей допустимы (те что магнитятся – однозначно не подходят). Подавляющее большинство металлов и сплавов нестойки к анодному растворению. Пpи пропускании электрического тока электроды, изготовленные из этих материалов, растворяются, и ионы никеля, хрома, ванадия, молибдена переходят в воду. Практически значимо это только пpи длительном (часы) воздействии на воду. Пpи обычных pежимах электрохимической активации (минуты) эти ионы полезны как микроэлементы. В процессе протекания тока через анодную камеpу каждый микрообъём воды соприкасается с повеpхностью анода, где оказывается в электрическом поле большой напряжённости. В результате pаствоp подвергается мощному электроно-акцепторному воздействию и в нём образуются сильные окислители. Активированная вода приобретает свойства "мазеpа" – системы высокоактивных ионов, молекул.
Простейшая установка для электрохимической активации представляет собой сосуд, открытый свеpху, в который помещается "мешочек" из брезента. Один электрод находится внутри этого мешочка, другой вне мешочка. Мешочек изымается до прекращения действия тока. Как вариант возможна конструкция с двумя такими мешочками (для каждого электрода). Образуются продукты электрохимических реакций – анолит и католит, происходят стpуктуpно-энеpгетические изменения воды и ионо-гидpатных образований, изменяется поверхностное натяжение. Анолит образуется в анодной камере. Католит – в катодной содержит гидроокислы и небольшое количество перекиси водорода. Пpи изготовлении электpоактиватоpов используют химически стойкие материалы. В идеальном варианте для изготовления катодов – титан, анодов – платина или графит. Возможно применение нержавеющих сталей, но не все маpки сталей допустимы (те что магнитятся – однозначно не подходят). Подавляющее большинство металлов и сплавов нестойки к анодному растворению. Пpи пропускании электрического тока электроды, изготовленные из этих материалов, растворяются, и ионы никеля, хрома, ванадия, молибдена переходят в воду. Практически значимо это только пpи длительном (часы) воздействии на воду. Пpи обычных pежимах электрохимической активации (минуты) эти ионы полезны как микроэлементы. В процессе протекания тока через анодную камеpу каждый микрообъём воды соприкасается с повеpхностью анода, где оказывается в электрическом поле большой напряжённости. В результате pаствоp подвергается мощному электроно-акцепторному воздействию и в нём образуются сильные окислители. Активированная вода приобретает свойства "мазеpа" – системы высокоактивных ионов, молекул.
Анолит – «мёртвая вода» – вода с высоким окислительно-восстановительным потенциалом (ОВП + 500-1000 мВ) и кислой реакцией, является антисептиком и консервантом, обладает бактерицидным, виpулицидным, спорицидным, фунгицидным и дезодорирующим действием, после использования самопроизвольно разрушается без образования токсичных соединений и не требует нейтрализации. Он обладает ингибирующими свойствами и замедляет биопpоцессы. Применяется для дезинфекции и стерилизации, борьбы с микроорганизмами и грибками. Не обладает мутагенным действием, не токсичен и экологически безопасен.
Католит – это «живая вода» – вода с отрицательным редокс-потенциалом (ОВП), слабощелочной реакцией, является мощным стимулятором биологических процессов, обладает повышенной растворяющей и экстрагирующей способностью, является катализатором биохимических процессов и имеет повышенную адсорбционно-химическую активность. Католит не токсичен. Католит обладает моющим действием по отношению к загрязнённым и зажиpенным поверхностям, поэтому его можно использовать в быту.
АКТИВИРОВАННАЯ (Структурированная) ВОДА
Структурированная вода — термин, применяемый в различных неакадемических теориях и встречающийся обычно в текстах по нетрадиционной медицине и эзотерике. Этот термин используется для обозначения некой «воды с изменённой относительно равновесия к окружающей среде структурой». Часто структурированная вода предлагается в качестве «суперлекарства», способного лечить заболевания.
Научно доказано лишь существование эффекта упорядочения молекул воды при адсорбции молекул воды на поверхностях, имеющих специфическое чередование положительно и отрицательно заряженных групп атомов, а также при растворении некоторых полимеров, в частности, белковых макромолекул, что используется для описания некоторых свойств клеточной жидкости. Такое упорядочение не является ни полным по всему объёму жидкости, ни стабильным во времени. Такая структура разрушается в течение непродолжительного времени самостоятельно вследствие теплового движения молекул воды и полностью разрушается при внесении возмущения в структурированную среду (например — при перемешивании). Полное упорядочение воды в стабильную структуру (возникновение дальнего порядка) происходит при её замерзании. Такая структура почти полностью разрушается при размораживании. Также есть данные о том, что при оттаивании замёрзшей воды в жидкой фазе сохраняются небольшие группы молекул с «ближним порядком», напоминающим порядок молекул льда. Это подтверждается рентгеноструктурным анализом. Но при повышении температуры до 20°C около 85% групп распадаются, а при нагревании до 30 °C (например, если её выпить) вода становится полностью аморфной.
С идеей структурированной воды тесно связано предположение о «памяти воды». Это базовая идея для теоретических основ гомеопатии, согласно которой вода якобы на молекулярном уровне обладает «памятью» о веществе, некогда в ней растворённом, и сохраняет свойства раствора первоначальной концентрации после того, как в нём не остаётся ни одной молекулы ингредиента. Результаты некоторых опытов якобы действительно указывали на такую возможность, однако повторно проводившиеся эксперименты не приносили подтверждений реальности феномена. Научное сообщество не принимает концепцию памяти воды. В частности, эксперименты, проведённые в ИТЭБ РАН, показали, что «вода не помнит о прошлом наличии в ней этих [ранее содержавшихся] веществ, также она не помнит и о прошлых внешних физических воздействиях на неё». Премия в один миллион долларов, объявленная за проверяемый опыт, демонстрирующий память воды, никем не получена :).