Дмитрий Петров (Воронеж)
Наиболее важными параметрами воды для полива растений и существенно влияющими на их развитие являются кислотность, жёсткость и окислительно-восстановительный потенциал. Именно значения этих параметров делают воду подходящей либо неподходящей для кактусов и требуют измерения, а при необходимости и коррекции. Помимо понимания роли каждого из названных параметров, необходимо понимание их всего лишь относительной взаимосвязи. Довольно часто приходится слышать мнение о неразрывной связи кислотности и жёсткости, которое можно выразить формулой: «мягкое = кислое, жёсткое = щелочное». Для опровержения можно привести несколько примеров:
Пример 1: раствор соды – гидрокарбоната натрия. Реакция – выраженная щелочная т.к. pH>10,0 а вот жёсткость равна нулю, потому, что в растворе нет катионов, образующих соли жёсткости.
Пример 2: Гипс, является сульфатом кальция (CaSO4·2H2O). Хотя и плохо растворим в воде, содержит катионы кальция, которые определяют жёсткость. Но гипс имеет слабо-кислую реакцию (pH=5,5) так как является солью щелочноземельного металла и сильной кислоты.
КИСЛОТНОСТЬ (pH)
Кислотность – свойство воды и растворов, выражающееся водородным показателем, и обозначаемое pH. Это мера активности ионов водорода в растворе, вычисляемая как взятый с обратным знаком десятичный логарифм активности водородных ионов, выраженной в молях на один литр:
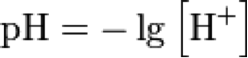
Содержание ионов водорода (гидроксония – H3O+) в природных водах больше всего определяется соотношением концентраций угольной кислоты и её ионов:
CO2 + H20 ⇔ H+ + HCO3– ⇔ 2 H+ + CO32-.
При диссоциации гидрокарбонатов Ca(HCO3)2 и Mg(HCO3)2 также образуются ионы НСО3–. Увеличение их концентрации ведёт к увеличению рН вследствие гидролиза. Для поверхностных вод характерна слабощелочная реакция. Изменения величины рН тесно связаны с процессами фотосинтеза (из-за потребления СО2 водной растительностью) и распада органических веществ. Источником ионов водорода являются также гуминовые кислоты, присутствующие в кислых почвах, перегное и болотных водах. Концентрация ионов водорода подвержена сезонным колебаниям. Зимой рН для большинства речных вод составляет 6,8-7,4, летом 7,4-8,2.
|
Показатель
|
Единицы измерения
|
WHO (всемирная организация здравоохранения)
|
USEPA (США)
|
ЕС (Европа)
|
СанПиН (Россия)
|
|
Водородный показатель
|
рН
|
Не регламентировано
|
6.5 – 8.5
|
6.5 – 8.5
|
6 – 9
|
ИССЛЕДОВАНИЕ КИСЛОТНОСТИ ВОДЫ
Единицы измерения.
Так как в кислых растворах [H+] > 10−7, то у кислых растворов pH < 7, аналогично, у щелочных растворов pH > 7, pH нейтральных растворов равен 7.
Способы измерения.
1. Самым простым, наиболее распространённым, но не очень точным является индикаторный метод измерения кислотности. Для этого используются кислотно-основные индикаторы — органические вещества-красители, цвет которых зависит от pH среды. К наиболее известным индикаторам принадлежат лакмус, фенолфталеин, метиловый оранжевый (метилоранж) и другие. Индикаторы способны существовать в двух по-разному окрашенных формах — либо в кислотной, либо в основной. Изменение цвета каждого индикатора происходит в своём интервале кислотности, обычно составляющем 1–2 единицы. Для расширения рабочего интервала измерения pH используют так называемый универсальный индикатор, представляющий собой смесь из нескольких индикаторов. Универсальный индикатор последовательно меняет цвет с красного через жёлтый, зелёный, синий до фиолетового при переходе из кислой области в щелочную. Определения pH индикаторным методом затруднено для мутных или окрашенных растворов.

2. Использование специального прибора — pH-метра — позволяет измерять pH в более широком диапазоне и более точно (до 0,01 единицы pH), чем с помощью индикаторов.




Ионометрический метод определения pH основывается на измерении милливольтметром-ионометром ЭДС гальванической цепи, включающей специальный стеклянный электрод, потенциал которого зависит от концентрации ионов H+ в окружающем растворе и хлорсеребрянный электрод сравнения. Способ отличается удобством и высокой точностью, особенно после калибровки индикаторного электрода в избранном диапазоне рН, позволяет измерять pH непрозрачных и цветных растворов. В отличие от лабораторных (прецизионных) pH-метров бытовые измерители pH не обладают столь высокой точностью, но позволяют быстро проводить измерения, они удобны для полевых условий. Некоторые pH-метры рассчитаны на измерение кислотности почв. Обычно pH-метры требуют калибровки с помощью буферного раствора с точно известным pH. Для более точного измерения необходимо учитывать температуру.
3. Кислотно-основное титрование также даёт точные результаты определения кислотности растворов. Раствор известной концентрации (титрант) по каплям добавляется к исследуемому раствору. При их смешивании протекает химическая реакция. Точка эквивалентности — момент, когда титранта точно хватает, чтобы полностью завершить реакцию, — фиксируется с помощью индикатора. Далее, зная концентрацию и объём добавленного раствора титранта, вычисляется кислотность раствора. Метод очень точен, но громоздок, его невозможно применить в полевых условиях, требует точности при приготовлении титранта. Вряд ли возможно его применение в практике кактусовода- любителя.
ЖЁСТКОСТЬ
Как уже говорилось, жёсткость является одним из наиболее важных параметров воды для растений. И при этом жёсткость природной воды подвержена ещё большим колебаниям, чем кислотность. Жёсткость водопроводной воды зависит не только от источника водоснабжения, но и от времени года, атмосферных явлений и др. факторов.
В большинстве населённых пунктов водозабор осуществляется из рек, которые несут в себе воду изначально более или менее жёсткую. Воды различных рек по нарастанию жёсткости можно расположить в следующий ряд:
Нева – Енисей – Верх. Волга – Обь – Москва – Днепр – Дон – Нижн. Волга
Для целей кактусоводства наиболее подходит мягкая вода, и чем она мягче, тем меньше забот и хлопот у кактусовода и тем лучше чувствуют себя его растения. J Это связано со следующими обстоятельствами:
- жёсткость угнетает рост и развитие растений;
- соли жёсткости, накапливаясь у всасывающей поверхности корней, могут оседать на корневых волосках и вызывать их отмирание;
- соли жёсткости оседают на пористых компонентах субстрата и забивают поры, после чего субстрат теряет присущие ему свойства;
- соли жёсткости оседают на нижней части стебля, корневых шейках и колючках, ухудшая эстетику.
Всё это в большей степени касается временной (карбонатной) жёсткости, постоянная не настолько важна для растений.
Условно воду для полива можно ранжировать по пригодности следующим образом:

Здесь расчёт дан для результатов тестов с помощью TDS-метра, ниже приведены таблицы перевода в любые единицы измерения.
Возможен ли полив излишне жёсткой водой? Да, конечно, возможен. Но настолько долго, насколько хватит буферной ёмкости субстрата (если таковая имеется). Это можно пояснить на следующем примере:
если растения содержатся в субстрате с большой долей торфа (который поглощает соли жёсткости, и поэтому является буфером) и довольно часто пересаживаются то в течение одного-двух вегетационных сезонов вполне можно использовать для полива практически любую, в том числе и жёсткую воду. Торф при этом НЕ должен быть нейтрализованным.
Чем меньше буферных компонентов содержит субстрат, тем важнее полив более мягкой водой. Это же касается и случаев редкой пересадки, когда либо кактусисту не хватает времени на более частые пересадки, либо когда растения некоторых родов не любят частых манипуляций с их корневой системой, например, ариокарпусы.
Единицы измерения.
Для численного выражения жёсткости воды указывают концентрацию в ней катионов кальция и магния. Рекомендованная единица СИ для измерения концентрации — моль на кубический метр (моль/м³), однако, на практике для измерения жёсткости используются градусы жёсткости и миллиграмм-эквиваленты на литр (мг-экв/л). В СССР до 1952 года использовали градусы жёсткости, совпадавшие с немецкими. В России для измерения жёсткости иногда использовалась нормальная концентрация ионов кальция и магния, выраженная в миллиграммах эквивалента на литр (мг-экв/л). Один мг-экв/л соответствует содержанию в литре воды 20,04 миллиграмм Ca2+ или 12,16 миллиграмм Mg2+ (атомная масса делённая на валентность).
С 1 января 2005 года в России введен новый Национальный стандарт Российской Федерации ГОСТ Р 52029-2003 «Вода. Единица жесткости»[1]. По новому ГОСТу жесткость выражается в градусах жесткости (°Ж). 1 °Ж соответствует концентрации щелочноземельного элемента, численно равной 1/2 его милимоля на литр (1 °Ж = 1 мг-экв/л).Иногда указывают концентрацию, отнесённую к единице массы, а не объёма, особенно, если температура воды может изменяться или если вода может содержать пар, что приводит к существенным изменениям плотности.
В разных странах использовались (и используются до сих пор) различные внесистемные единицы — градусы жёсткости.
|
Градус |
Обозначение
|
Определение
|
Величина
|
|
°Ж
|
ммоль/л
|
|
Немецкий
|
°dH (degrees of hardness),
°dGH ((German Hardness) для общей жёсткости),
°dKH (для карбонатной жёсткости)
|
1 часть оксида кальция (СаО) или 0.719 частей оксида магния (MgO) на 100 000 частей воды (или 10 мг СаО в 1 л воды, или 7.194 мг MgO в 1 л воды)
|
0,3566
|
0,1783
|
|
Английский
|
°e (Clark)
|
1 гран (0.0648 г) CaCO3 на 1 английский галлон (4.546 л) воды
|
0,2848
|
0.1425
|
|
Французский
|
°TH
|
1 часть CaCO3 на 100 000 частей воды
|
0,1998
|
0,0999
|
|
Американский
|
Ppm
|
1 часть CaCO3 на 1 000 000 частей воды (1мг CaCO3 в 1 л воды)
|
0,0200
|
0,0100
|
Английские, французские и американские градусы жесткости выражают содержание карбоната кальция (СаСО3), в то время как немецкие градусы показывают содержание окиси кальция (СаО).
Таблица перевода величин:
|
Единицы |
Мг-экв/л
|
Градусы жёсткости
|
|
немецкий
|
французский
|
американский
|
английский
|
|
1 мг-экв/л
|
1
|
2.804
|
5.005
|
50.045
|
3.511
|
|
1 немецкий градус dH
|
0.3566
|
1
|
1.785
|
17.847
|
1.253
|
|
1 французский градус
|
0.1998
|
0.560
|
1
|
10,000
|
0.702
|
|
1 американский градус
|
0.0200
|
0.056
|
0.100
|
1
|
0.070
|
|
1 английский градус
|
0.2848
|
0.799
|
1.426
|
14.253
|
1
|
Способы измерения.
Определение временной (KH, карбонатной, устранимой) жёсткости воды.
Временная жёсткость связана с присутствием в воде наряду с катионами Ca2+ и Mg2+ гидрокарбонатных или бикарбонатных анионов (HCO3-). При кипячении воды, гидрокарбонатные анионы вступают в реакцию с этими катионами и образуют с ними очень мало растворимые карбонатные соли, которые выпадают в осадок. На примере ионов кальция эта реакция выглядит так: Ca2+ + 2HCO3– = CaCO3↓ + H2O + CO2↑
Если исходить из определения карбонатной жесткости то её корректное измерение должно быть основано на кипячении заданного объема воды с последующим взвешиванием образовавшегося осадка (накипи), но на практике сделать это трудно, поэтому используют более лёгкий метод – титрование соляной кислотой. Титрование – это добавление в исследуемую пробу раствора реагента, концентрация которого заранее известна. По расходу этого реагента – он взаимодействует с тем веществом, содержание которого хотят определить, рассчитывают концентрацию определяемого вещества.
Титрование соляной кислотой
Реактивы:
- Раствор соляной кислоты HCl 0,05М. Для приготовления 4 мл. покупной соляной кислоты (38%) добавляют в 100-20 мл. дистилированной воды (кислоту в воду! а не наоборот!) и доводят объём до 1 литра.
- Индикатор метилоранж (неточное количество «на кончике ножа» растворяют в 100 мл. дистиллированной воды.
Анализ:
Точно отмеряем 50 мл. исследуемой воды, добавляем 5-10 капель р-ра индикатора (цвет стал жёлтым, напоминает светлое пиво ) . Помешивая, из шприца добавляем в воду раствор кислоты, в какой-то момент от одной капли (!) произойдёт резкое изменение окраски с жёлтой на оранжевую, напоминающую по цвету «Фанту».



Формула реакции: H+ + HCO3– <–> H2CO3 <–> CO2 + H2O т.е. ионы водорода реагируют вовсе не с ионами кальция, а с гидрокарбонатными ионами, и как только они заканчиваются pH среды резко смещается в кислую сторону и изменяет окраску индикатора на оранжевую.
Результат:
Карбонатная жесткость в мг-экв/л будет численно равна объему кислоты (в мл), израсходованному для титрования. Для иных объёмов формула расчёта: Жесткость карбонатная(мг-экв/л) = (1000*Скислоты*Vкислоты):Vводы , где Скислоты – концентрация кислоты в молях (М/л), Vкислоты – объем раствора кислоты использованный при титровании (мл), Vводы – объем пробы воды, взятой для титрования (мл).
Пример:
На титрование ушло 2 мл. р-ра кислоты. Это означает, что карбонатная жёсткость исследуемой волды равна 2.0 мг-экв/л. Для перевода в градусы KH значение в мг-экв/л надо умножить на 2.804, получим 2.0 * 2.804 = 5,6°KH.
Поскольку данная реакция по принципу является реакцией нейтрализации, то она же может быть условно использована для определения pH (учитывая, что момент перехода равен примерно pH 4,0).
Определение общей жёсткости воды.
Наибольшая точность измерения достигается комплексонометрическим титрованием трилоном Б, в буферном растворе на индикаторах эриохром черный Т или кислотный хром темно-синий. Но для наших целей особо точное измерение не требуется, поэтому мы обратимся к более простым способам измерения общей жёсткости.
Использование жидкого теста из зоомагазина
 Определение очень простое и быстрое. На примере теста «Sera gH test».
Определение очень простое и быстрое. На примере теста «Sera gH test».
В мерный стаканчик надо набрать 5 мл исследуемой воды, далее в достаточно освещённом помещении, поместив стаканчик против белого фона, надо по каплям добавлять реагент в воду. После каждой капли стаканчик надо встряхивать. Количество капель подсчитывать. Прекращение титрования при при смене цвета на зелёный. Число потраченных капель и будет жёсткостью воды, выраженной в немецких градусах. Стоит отметить, что в зависимости от значения общей жёсткости переход цвета может происходить путём разных последовательных цветовых переходов. Более мягкая вода будет переходить от бесцветной к зелёной окраске так:
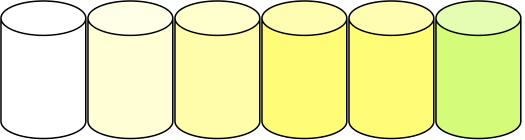
это была вода общей жёсткостью 5°dGH, более жёсткая вода даёт другой цветовой переход, и конечный цвет более интенсивен:
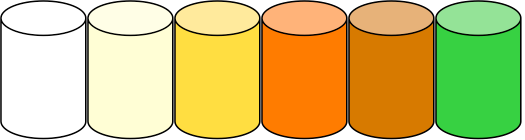
здесь тестировалась вода с жёсткостью 12° dGH.
Недостатками магазинных тестов для определения общей жёсткости являются их относительная дороговизна и большая (до 25%) погрешность.
Использование индикатора
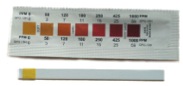 Реализована также и «бумажная» версия индикатора в виде тест-полосок для количественного определения общей жёсткости. При очевидном удобстве использования у этого метода имеются и недостатки, это высокая стоимость, большая погрешность (до 20%), кроме того такие тесты редко можно встретить в продаже.
Реализована также и «бумажная» версия индикатора в виде тест-полосок для количественного определения общей жёсткости. При очевидном удобстве использования у этого метода имеются и недостатки, это высокая стоимость, большая погрешность (до 20%), кроме того такие тесты редко можно встретить в продаже.
Использование кондуктометра
Кондуктометрический анализ основан на изменении концентрации вещества или химического состава среды в межэлектродном пространстве; он не связан с потенциалом электрода, который обычно близок к равновесному значению. По сути кондуктометрия – есть измерение электропроводности. Этот метод позволяет дать приблизительную оценку общей жёсткости, при наличии кондуктометра измерение занимает практически несколько секунд.
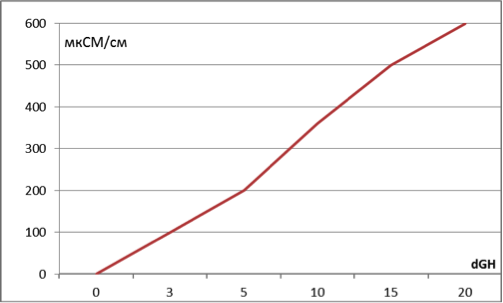
По электропроводности легко установить примерное значение общей жёсткости.
 Жёсткость пресной, неминерализованной воды легко и быстро можно определить с помощью TDS-метра или солемера. Метод не обладает лабораторной точностью, но для нужд кактусовода более чем достаточен. В быту этот прибор чаще всего используется для оценки качества работы фильтров для воды или определения необходимости замены картриджа фильтра. Сокращение TDS означает Total Dissolved Solids (TDS) – «общее количество растворенных частиц», это справедливо отражает то, что при измерении учитываются все вещества, а не только кальций и магний. Однако, в простой пресной воде именно они преобладают. Единицей измерения может выступать ppm (parts per million) – в частицах на миллион частиц воды. Соотношение между единицами измерения в мг/л и ppm почти равное и для простоты можно принять, что 1 мг/л = 1 ppm. При использовании кондуктометра, отградуированного в мкС/см используется коэффициент 0,75 ( мкС/см х 0.75 = TDS мг/л). В бытовых условиях использование TDS-метра – это, пожалуй, наиболее практичный и простой метод исследования жёсткости.
Жёсткость пресной, неминерализованной воды легко и быстро можно определить с помощью TDS-метра или солемера. Метод не обладает лабораторной точностью, но для нужд кактусовода более чем достаточен. В быту этот прибор чаще всего используется для оценки качества работы фильтров для воды или определения необходимости замены картриджа фильтра. Сокращение TDS означает Total Dissolved Solids (TDS) – «общее количество растворенных частиц», это справедливо отражает то, что при измерении учитываются все вещества, а не только кальций и магний. Однако, в простой пресной воде именно они преобладают. Единицей измерения может выступать ppm (parts per million) – в частицах на миллион частиц воды. Соотношение между единицами измерения в мг/л и ppm почти равное и для простоты можно принять, что 1 мг/л = 1 ppm. При использовании кондуктометра, отградуированного в мкС/см используется коэффициент 0,75 ( мкС/см х 0.75 = TDS мг/л). В бытовых условиях использование TDS-метра – это, пожалуй, наиболее практичный и простой метод исследования жёсткости.
Использование электролизера
 Для грубой, неколичественной оценки качества воды для полива может быть использован простой недорогой прибор – электролизер. Исследование занимает меньше минуты, для этого одна пара электродов погружается в исследуемую воду, а вторая пара – в дистиллированную или очищенную обратным осмосом. Если исследуемая вода содержит большое количество примесей то наступает электрохимическая реакция с материалом электродов, вода при этом приобретает сине-зелёный оттенок, а у её поверхности образуется более интенсивно окрашенный слой, чем больше в воде катионов солей жёсткости тем интенсивнее окраска. Чистая вода в ёмкости сравнения либо не изменяется внешне либо приобретает кремоватую или оранжеватую окраску.
Для грубой, неколичественной оценки качества воды для полива может быть использован простой недорогой прибор – электролизер. Исследование занимает меньше минуты, для этого одна пара электродов погружается в исследуемую воду, а вторая пара – в дистиллированную или очищенную обратным осмосом. Если исследуемая вода содержит большое количество примесей то наступает электрохимическая реакция с материалом электродов, вода при этом приобретает сине-зелёный оттенок, а у её поверхности образуется более интенсивно окрашенный слой, чем больше в воде катионов солей жёсткости тем интенсивнее окраска. Чистая вода в ёмкости сравнения либо не изменяется внешне либо приобретает кремоватую или оранжеватую окраску.
ОВП (Редокс, окислительно-восстановительный потенциал, Eh )
Окислительно-восстановительный потенциал (Eh) является одной из важных характеристик состояния природных вод. Он в значительной степени определяет геохимическую подвижность элементов с переменной валентностью и формы их миграции. Природные воды содержат в себе разновалентные ионы и нейтральные молекулы одного и того же элемента, которые и составляют отдельную окислительно-восстановительную систему. Совместное существование ряда таких систем приводит к установлению некоторого подвижного равновесного состояния, определяющего ОВП воды.
Вклад отдельных систем в окислительно-восстановительное состояние природных вод неодинаков. Окислительно-восстановительные системы, влияние которых на общий ОВП среды преобладает являются потенциалопределяющими. Таких систем несколько. Главные из них образуются за счёт кислорода, соединений железа, серы различных валентностей и некоторых органических веществ.
Кислород является наиболее универсальным окислителем. Даже небольшие его количества заметно влияют на величину Eh, при повышении концентрация кислорода в воде величина Eh также увеличивается и может достигать +700 мВ.
Сера, обладающая способностью менять валентность от 2 до 6 играет особую роль в формировании ОВП воды, наличие сероводорода снижают ОВП до -100 мВ и ниже.
Железо – один из распространённых элементов в природных водах. Окисленная трехвалентная форма железа очень легко подвержена гидролизу и при значениях рН, характерных для природных вод, возможное содержание иона Fe (III) в растворе обычно невелико и составляет десятые и сотые доли миллиграмма в литре, тогда как концентрация иона Fe (II) может достигать нескольких граммов в литре. Поэтому значение ОВП системы железа (Fe3+ <> Fe2+) в большой степени зависит от рН среды, резко снижаясь при повышении рН.
В природной воде ОВП изменяется от -500 до +700 мВ. Поверхностные и грунтовые воды, содержащие свободный кислород обычно имеют положительный Eh от 100 до 500 мВ. Подземные воды, связанные с нефтяными залежами всегда имеют отрицательный Eh до -500 мВ . Природные источники воды с отрицательным ОВП встречаются редко.
Активность электронов является важнейшей характеристикой внутренней среды любого организма. Практически все биологически важные системы, определяющие аккумуляцию и потребление энергии, репликацию и передачу наследственных признаков, всевозможные ферментативные системы организма, содержат молекулярные структуры с разделенными зарядами.
Внутренние среды живых организмов находятся в восстановленном состоянии. ОВП, измеренный платиновым электродом относительно хлорсеребряного электрода сравнения обычно находится в пределах от +100 до – 200 mV. В то же время ОВП обычной воды (вода из под крана, питьевая вода в бутылках и пр.), измеренный таким же способом, практически всегда больше нуля и обычно находится в пределах от +100 до +400 mV. Это означает, что активность электронов во внутренней среде намного выше, чем активность электронов в воде. Необходимое изменение ОВП воды при всасывании происходит за счет затраты электрической энергии клеточных мембран, т.е. энергии самого высокого уровня, энергии, которая фактически является конечным продуктом биохимической цепи трансформации питательных веществ. Количество энергии, затрачиваемой организмом на достижение биосовместимости воды, пропорционально ее количеству и разности ОВП воды и внутренней среды организма. Если вода имеет ОВП близкий к значению ОВП внутренней среды организма, то электрическая энергия клеточных мембран (жизненная энергия организма) не расходуется на коррекцию активности электронов воды и она быстро усваивается, поскольку обладает биологической совместимостью по этому параметру.
Когда значение ОВП положительно, то свойства воды окислительные. Такие показатели наиболее часто встречаются в поверхностных водах. Чем выше положительный ОВП тем более выражены окислительные свойства воды, а при достижении величин Eh +800 до +1000 mV вода приобретает свойства антисептика. Контакт живых клеток с такой водой приводит к повреждению их мембран, а длительный контакт приводит к гибели клетки. Когда значение ОВП отрицательно, то свойства воды – восстановительные. Это типично для подземных горных источников, талой воды. Такая вода может являться источником энергии для живых клеток.
В познавательных целях ниже приведены обычные значения ОВП некоторых жидкостей ( mV )
Вода водопроводная +220 – +380
Вода бутилированная +200 – +400
Вода в колодцах, родниках, дождевая +200 – +320
Вода из скважины глубиной более 100м -50 – +50
Католит (используемый в лечебных целях) 0 – -1200
Анолит рН= 1-7 ( для дезинфекции) 0 – +1000
Свежий сок (с грядки) +30 – +70
Свежевыжатый сок (после суток хранения плодов) +50 – +100
Берёзовый сок (после двух суток хранения) -450
Тот же сок после кипячения +270
Слюна практически здорового человека -50 – +50
Материнское молоко -70
Внутренняя среда практически здорового человека -70
Оптимальная среда для подвижности сперматозоидов -130
ИССЛЕДОВАНИЕ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНОГО ПОТЕНЦИАЛА ВОДЫ
 Показатель ОВП определяет отношение компонентов «окислителей» к компонентам «восстановителям» и находится в прямой зависимости от этого отношения. Наибольшей окислительной способностью среди всех окислителей обладает кислород, а среди восстановителей – водород. Окислительно – восстановительный потенциал зависит от температуры и относительно взаимосвязан с рН.
Показатель ОВП определяет отношение компонентов «окислителей» к компонентам «восстановителям» и находится в прямой зависимости от этого отношения. Наибольшей окислительной способностью среди всех окислителей обладает кислород, а среди восстановителей – водород. Окислительно – восстановительный потенциал зависит от температуры и относительно взаимосвязан с рН.
ОВП при постоянной температуре зависит только от состава среды и может быть сообщён этой средой погруженному в неё электронному проводнику (электроду) , если между средой и электродом не нарушен электронный обмен. ОВП устойчив, если среда содержит заметные количества окислителя и восстановителя. При этом первый есть продукт окисления второго. Значение ОВП для каждой окислительно-восстановительной реакции может иметь как положительное, так и отрицательное значение. При положительном ОВП – вода захватывает и присоединяет электроны тех веществ, с которыми вступает в реакцию (окисляет), а при отрицательном – отдает электроны (восстанавливает).
ОВП обозначается как Eh и выражается в милливольтах (мВ). Для измерения ОВП применяют ОВП-метры (ОRP или редокс-метры) с различными электродами. Благодаря компактным размерам, простоте применения, скорости работы и относительной дешевизне ОВП-метры могут применяться для оперативного выявления ОВП питьевых и других вод. ОВП-метр показывает количество мВ, затраченных на отрыв электронов от исследуемой воды. Чем более восстановлена вода, тем легче она отдает электроны, тем значение ОВП меньше. Приборы для измерения ОВП (ORP) заметно дороже pH- и TDS-метров. Однако замены им нет, так как химических тест-наборов или индикаторной бумаги для определения этого важного параметра не существует.