Дмитрий Петров (Воронеж)
Какой водой чаще всего поливают кактусы?
- Обычная водопроводная вода.
На территории России и СНГ эта вода чаще всего излишне жёсткая, хлорирована и чаще всего имеет сдвиг pH в щелочную сторону. Если другие источники воды для полива недоступны то свойства так ой воды можно улучшить отстаиванием в затемнённом месте или непрозрачной посуде или опусканием на сутки в воду мешочка с торфом. Этот старый метод позволяет и смягчить и подкислить воду.
Может быть с успехом применена при условии её сбора в экологически благополучных регионах, в противном случае такая вода может действовать на растения губительно. В промышленно развитых регионах дождевая вода, особенно после длительного отсутствия осадков, может содержать не только серную и сернистую кислоты, но и множество других вредных для растений веществ. Важен и метод сбора, дождевая вода, собранная с гудроновых или цинковых крыш не обладает оптимальными для растений свойствами, и вред может превысить пользу.
Содержит продукты жизнедеятельности рыб и других обитателей аквариума. Многие любители отмечают хорошие результаты при поливе водой из аквариума. Но следует помнить о том, что качество и пригодность этой воды зависят от многих условий – объёма самого аквариума, числа, размеров и видов рыб его населяющих, количества водных растений в аквариуме, состояния фильтров, заселённости водорослями и, наконец, от частоты замены воды. Проблемы при использовании аквариумной воды могут возникнуть из-за дисбаланса по минеральным элементам. Обычно аквариумная вода содержит избыточное количество нитратов и фосфатов, их источником являются продукты жизнедеятельности рыб (ракообразных, улиток). Водные растения потребляют и фосфаты и нитраты, но обычно они не могут уменьшить их содержание до приемлемого уровня. Если фосфаты аквариумной воды могут быть полезны кактусам, то с нитратами дело обстоит хуже – в избытке они нарушают правильное развитие суккулентных растений. При этом аквариумная вода практически не содержит калия и микроэлементов, что тоже является её существенным недостатком.
- Дистиллированная вода и вода, очищенная обратным осмосом.
Полив дистиллированной или очищенной обратным осмосом водой не является дешёвым удовольствием, однако, если стоимость системы поделить на объём воды то заоблачных цифр не будет. А если добавить к этому то обстоятельство, что такая система может использоваться как источник питьевой воды то приобретение системы обратного осмоса может стать и вовсе оправданным. Такая вода свободна ненужных растениям катионов солей жёсткости, не содержит натрия, хлоридов, но вместе с тем не содержит и столь необходимых минеральных элементов как калий, фосфор, микроэлементы. Для того, чтобы такая вода была близка к идеалу в неё необходимо внести нужные ионы. Сделать это можно двумя способами:
- С использованием минерализатора.

Если система обратного осмоса используется как источник воды для питья и приготовления пищи то применение минерализатора просто обязательно т.к. из воды практически полностью удаляются необходимые человеческому организму соли, и качественно очищенная вода, как и дистиллят не обеспечивают организм человека и животных теми веществами, которые им необходимы. Но параметры «полезности» воды для организма человека и растительного организма сильно отличаются друг от друга. Обогащение воды ионами кальция и, в меньшей степени, магния и натрия полезно для нашего организма, но растениям такого количества ионов не требуется.
- Внося в воду заданное количество минералов в пропорциях,
 учитывающих физиологические особенности суккулентов. Этот вариант даёт возможность соблюсти нужное именно растениям количество и соотношение макро- и микроэлементов, в первую очередь калия и фосфора. Более того с помощью внесения готового минерального состава можно легко регулировать концентрацию либо менять пропорции в зависимости от сезонной потребности растений, а в некоторых ситуациях разумным решением может быть даже полив чистой водой без добавления минералов. Например, в конце вегетационного периода можно ограничиться добавлением только монофосфата калия.
учитывающих физиологические особенности суккулентов. Этот вариант даёт возможность соблюсти нужное именно растениям количество и соотношение макро- и микроэлементов, в первую очередь калия и фосфора. Более того с помощью внесения готового минерального состава можно легко регулировать концентрацию либо менять пропорции в зависимости от сезонной потребности растений, а в некоторых ситуациях разумным решением может быть даже полив чистой водой без добавления минералов. Например, в конце вегетационного периода можно ограничиться добавлением только монофосфата калия.
А нужна ли коррекция ?
Не стоит забывать, что на самом деле важен не столько показатель кислотности самой воды, сколько pH почвы (субстрата). Компоненты субстрата обладают ионообменной способностью, в почве совокупность этих свойств называется почвенным поглощающим комплексом. Компоненты субстрата при гравийной культуре также оказывают значительное влияние на pH раствора. Один или несколько компонентов могут обладать щелочной реакцией и значительной буферной ёмкостью, тогда для сдвига pH в кислую сторону требуется длительный полив подкисленной водой до исчерпания данного буфера. При попадании воды в почвенный субстрат образуется почвенный раствор, по свойствам отличающийся от простого раствора веществ в воде, так как в силу вступают физико-химические явления и процессы. Почвенный раствор содержит до 30% коллоидных частиц, которые проявляют буферные, влагоудерживающие и другие свойства, в совокупности создающие из смеси минеральных и органических веществ довольно сложную и саморегулирующуюся систему.
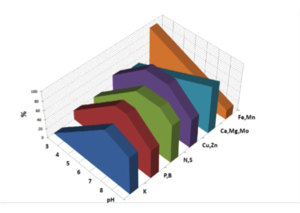 Кислотность субстрата влияет на растворимость, а также усвояемость растением различных минералов. В кислом субстрате лучше усваиваются микроэлементы – железо, бор, марганец. Наиболее значимые макроэлементы – фосфор и калий лучше усваиваются в слабокислой или нейтральной среде. Помимо этого для каждого вида суккулентов существует свой оптимальный диапазон кислотности почвы. Для большинства кактусов в условиях коллекции предпочтительной является слабокислая реакция субстрата. Многие виды родов Parodia s.l., Discocactus, Uebelmannia особо нетерпимо относятся к щелочной реакции, многие другие виды могут вполне хорошо себя чувствовать в довольно широком диапазоне кислотности субстрата.
Кислотность субстрата влияет на растворимость, а также усвояемость растением различных минералов. В кислом субстрате лучше усваиваются микроэлементы – железо, бор, марганец. Наиболее значимые макроэлементы – фосфор и калий лучше усваиваются в слабокислой или нейтральной среде. Помимо этого для каждого вида суккулентов существует свой оптимальный диапазон кислотности почвы. Для большинства кактусов в условиях коллекции предпочтительной является слабокислая реакция субстрата. Многие виды родов Parodia s.l., Discocactus, Uebelmannia особо нетерпимо относятся к щелочной реакции, многие другие виды могут вполне хорошо себя чувствовать в довольно широком диапазоне кислотности субстрата.
Прежде чем принять решение о коррекции каких-либо параметров воды и выборе метода необходимо осознать разницу условий произрастания в природе и в культуре. Время от времени снова и снова раздаётся интересный и очень важный для понимания физиологии суккулентов вопрос: Почему многие кактусы в местах произрастания прекрасно развиваются чуть ли не в чистом карбонате кальция при pH> 8, а в культуре нуждаются в мягкой и подкисленной воде для полива?
Для начала можем взглянуть на карту кислотности почв на примере Мексики, тем более что именно мексиканские виды чаще всего имеются в виду при такой постановке вопроса.
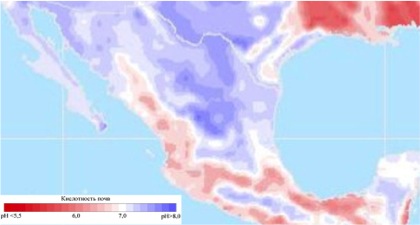
При просмотре этой карты возникают выводы:
- далеко не везде pH почвы имеет щелочную реакцию, в Южных и Юго-Западных штатах преобладают кислые почвы;
- даже там, где почвы щелочные, их pH очень редко превышает значение 7,5 то есть значения чаще всего близки к нейтральным.
- Сдвиг pH в щелочную сторону удивительным образом совпадает с местами произрастания наиболее эффектных кактусов (это мнение очень субъективно).
Также стоит помнить о существовании ризосферы. Ризосферой называют слой почвы, непосредственно контактирующий с корнями, который подвергается действию корневых выделений и является местом жизнедеятельности микроорганизмов. Кислотность в ризосфере может сильно отличаться от кислотности окружающей (основной) почвы. Это место обитания различных живых организмов – простейших, грибоподобных протист, нематод, которые питаются бактериями или отшелушивающимися клетками корня, а также грибов, при определённых условиях образующих микоризу – симбиотические отношения между грибом и корнем высшего растения. Стоит отметить, что для кактусов микориза является явлением факультативным, в аридных условиях встречается намного реже, чем в сельскохозяйственном производстве.
Существует ещё один аспект. Минералы, являющиеся солями кальция, могут сильно химически отличаться друг от друга даже при внешнем сходстве. Примером могут служить карбонат и сульфат кальция – мел и гипс. Мел имеет щелочную реакцию, а гипс – кислую, т.к. первый является солью слабой угольной кислоты, а второй – солью серной кислоты – одной из сильнейших кислот. Внешний вид в составе горной породы или грунта как мела, так и гипса может быть самым разным, он сильно зависит от сопутствующих элементов. На территории Мексики, особенно в северной её части сульфат кальция распространён значительно, часто в непосредственном соседстве с карбонатом кальция, но располагается чаще не на поверхности грунта, а на глубине от 20-30 см.
Присутствие в горных породах Мексики сульфата кальция в огромных количествах иллюстрируют селенитовые пещеры. Селенит – это кристаллическая разновидность гипса. Наиболее захватывающее зрелище представляет собой пещера Cueva de los Cristales, находящаяся в Чиуауа (Chihuahua). Огромные прозрачные кристаллы сульфата кальция природного происхождения достигают 11 метров в высоту.

Примечательно, что вода, связанная с этими пещерами всегда имеет выраженный отрицательный ОВП.
КОРРЕКЦИЯ КИСЛОТНОСТИ
Водопроводная вода в большинстве случаев имеет нейтральную или слабощелочную реакцию.
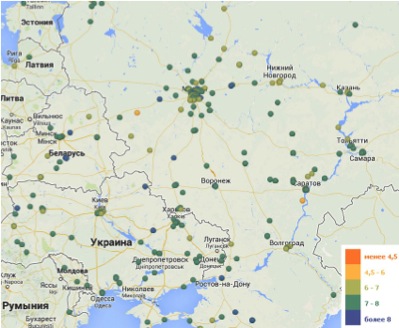
Для иллюстрации взята карта pH водопроводной воды с сайта http://www.aquafactor.ru/
Для большинства кактусов, особенно южноамериканских, лучшей является подкисленная вода, имеющая pH около 6,0. Обычно для подкисления используют различные органические и неорганические кислоты. В виду того, что кислоты при равной нормальности растворов имеют разную концентрацию ионов водорода нужно учитывать, что для снижения pH на единицу требуется разное количество кислоты.
|
Кислота
|
Нормальность раствора
|
pH
|
|
Лимонная / Citric
|
0.1н.
|
2.2
|
|
Лимонный сок / Lemon Juice
|
|
2
|
|
Ортофосфорная / Orthophosphoric
|
0.1 н.
|
1.5
|
|
Щавелевая / Oxalic
|
0.1 н.
|
1.3
|
|
Янтарная / Succinic
|
0.1н.
|
2.7
|
Эти и другие кислоты можно использовать для подкисления. Соляную и серную кислоты использовать нежелательно. Соляную по причине вредности для растений хлорид-иона, а серную по причине малой потребности в сульфат-ионах, которые начнут накапливаться). Фосфорная кислота и упомянутые в таблице карбоновые кислоты легко включаются в метаболизм растения.
КОРРЕКЦИЯ ЖЁСТКОСТИ (умягчение)
Термоумягчение (кипячение).
Основан на кипячении воды, в результате термически нестойкие гидрокарбонаты кальция и магния разлагаются с образованием накипи:
Ca(HCO3)2 → CaCO3↓ + CO2 + H2O.
 Такой метод нередко применяется в быту, возможно его применение и в кактусоводстве при недоступности других методов смягчения. При использовании метода необходимо продолжительное, не менее 30 минут кипячение, затем отстаивание в течение суток, после чего воду не взбалтывая, аккуратно сливают с осадка.
Такой метод нередко применяется в быту, возможно его применение и в кактусоводстве при недоступности других методов смягчения. При использовании метода необходимо продолжительное, не менее 30 минут кипячение, затем отстаивание в течение суток, после чего воду не взбалтывая, аккуратно сливают с осадка.
|
Преимущества метода
|
Недостатки метода
|
- Дешевизна (относительно цен на ЭН)
- Одновременно происходит стерилизация
|
- Устраняет только временную (карбонатную) жёсткость
- Требуется химически инертная и термостойкая посуда (чаще эмалированная)
- Требуется время на охлаждение, отстаивание и последующий слив
|
Если преобладает временная жёсткость, то этот способ позволяет получить вполне приемлемую по жёсткости воду. В воде, слитой с осадка, жёсткость представлена растворимыми солями, и если они присутствуют в умеренных количествах то растения к ним более терпимы, чем к солям временной жёсткости. Если же гидрокарбонатов в воде мало, то кипячение почти не влияет на жёсткость.
Частичное замораживание.
 Метод основан на образовании кристаллической решётки при замерзании воды в неподвижной среде. В кристаллическую решётку не включаются ионы щелочных и щелочноземельных металлов, а также анионы кислотных остатков. В результате вода, находящаяся в слое льда, является более чистой и более мягкой, чем остальная масса.
Метод основан на образовании кристаллической решётки при замерзании воды в неподвижной среде. В кристаллическую решётку не включаются ионы щелочных и щелочноземельных металлов, а также анионы кислотных остатков. В результате вода, находящаяся в слое льда, является более чистой и более мягкой, чем остальная масса.
Для получения мягкой воды этим способом вода наливается в ёмкость с большой площадью поверхности, ёмкость оставляется в среде с отрицательной температурой, например, на улице зимой. Важно, чтобы ёмкость стояла неподвижно. При замерзании 20-25% воды лёд убирают, а остальную воду выливают, она больше не понадобится. При таянии полученного льда образуется довольно чистая и мягкая вода.
|
Преимущества метода |
Недостатки метода
|
- Дешевизна
- Достаточное качество смягчения и очистки
|
- Требует специальной ёмкости
- Требуется время на замерзание и последующее оттаивание
- Легко реализуется в сезон, когда вода нужна меньше всего.
|
В нашем климате с октября по апрель большинство кактусов находятся в состоянии зимней стагнации – «на зимовке», когда полив подавляющего большинства сведён к нулю. В этом заключена причина непопулярности этого доступного и простого метода среди любителей кактусов.
Реагентное умягчение.
 Такой метод умягчения начинался с добавления в воду кальцинированной соды Na2CO3 или гашёной извести Ca(OH)2. При этом соли кальция и магния переходят в нерастворимые соединения и, как следствие, выпадают в осадок. Так, при добавлении гашёной извести происходит перевод «жёстких» солей кальция в нерастворимый карбонат:
Такой метод умягчения начинался с добавления в воду кальцинированной соды Na2CO3 или гашёной извести Ca(OH)2. При этом соли кальция и магния переходят в нерастворимые соединения и, как следствие, выпадают в осадок. Так, при добавлении гашёной извести происходит перевод «жёстких» солей кальция в нерастворимый карбонат:
Ca(HCO3)2 + Ca(OH)2 → 2CaCO3↓ + 2H2O
Часто используемым реагентом для устранения общей жесткости воды является ортофосфат натрия Na3PO4, входящий в состав большинства препаратов бытового и промышленного назначения:
3Ca(HCO3)2 + 2Na3PO4 → Ca3(PO4)2↓ + 6NaHCO3
3MgSO4 + 2Na3PO4 → Mg3(PO4)2↓ + 3Na2SO4
Ортофосфаты кальция и магния очень плохо растворимы в воде, поэтому легко отделяются механическим фильтрованием.
Применение указанных реагентов приводит к накоплению в воде одновалентных катионов и существенно увеличивает pH, что делает воду неподходящей для полива растений.
Использование щавелевой кислоты
 Поэтому для реагентного умягчения в целях кактусоводства используют другие вещества, такие как Трилон-Б (ЭДТА) или щавелевую кислоту. При использовании реагентов всегда необходимо их точное дозирование, для чего очень важно точно знать параметры жёсткости. По сложившейся практике наиболее часто используют щавелевую кислоту. Чистая щавелевая кислота – белое кристаллическое вещество, для её использования стоит приготовить её раствор заданной и точной концентрации, который добавляется в воду в точной пропорции (мл/л). После добавления щавелевой кислоты происходит выпадение осадка оксалата кальция. Обработанной воде необходимо отстояться, после чего воду аккуратно сливают с осадка.
Поэтому для реагентного умягчения в целях кактусоводства используют другие вещества, такие как Трилон-Б (ЭДТА) или щавелевую кислоту. При использовании реагентов всегда необходимо их точное дозирование, для чего очень важно точно знать параметры жёсткости. По сложившейся практике наиболее часто используют щавелевую кислоту. Чистая щавелевая кислота – белое кристаллическое вещество, для её использования стоит приготовить её раствор заданной и точной концентрации, который добавляется в воду в точной пропорции (мл/л). После добавления щавелевой кислоты происходит выпадение осадка оксалата кальция. Обработанной воде необходимо отстояться, после чего воду аккуратно сливают с осадка.
|
Преимущества метода
|
Недостатки метода
|
|
|
- Требует большой точности
- Требуется время на выпадение осадка
- Из-за колебаний жёсткости требуется частое измерение показателей жёсткости
- Магниевая жёсткость остаётся по причине растворимости оксалата магния.
|
Катионирование.
 Метод основан на использовании ионообменной гранулированной загрузки (чаще всего ионообменные смолы). Такая загрузка при контакте с водой поглощает катионы солей жёсткости (кальций и магний, железо и марганец). Взамен, в зависимости от ионной формы, отдавая ионы натрия или водорода. Эти методы соответственно называются Na-катионирование и Н-катионирование. При правильно подобранной ионообменной загрузке жёсткость воды снижается при одноступенчатом натрий-катионировании до 0,05-0,1 °Ж, при двухступенчатом — до 0,01 °Ж. В промышленности с помощью ионообменных фильтров заменяют ионы кальция и магния на ионы натрия и калия, получая мягкую воду. Для получения воды, пригодной для полива растений допустимо использование только Н-катионитов.
Метод основан на использовании ионообменной гранулированной загрузки (чаще всего ионообменные смолы). Такая загрузка при контакте с водой поглощает катионы солей жёсткости (кальций и магний, железо и марганец). Взамен, в зависимости от ионной формы, отдавая ионы натрия или водорода. Эти методы соответственно называются Na-катионирование и Н-катионирование. При правильно подобранной ионообменной загрузке жёсткость воды снижается при одноступенчатом натрий-катионировании до 0,05-0,1 °Ж, при двухступенчатом — до 0,01 °Ж. В промышленности с помощью ионообменных фильтров заменяют ионы кальция и магния на ионы натрия и калия, получая мягкую воду. Для получения воды, пригодной для полива растений допустимо использование только Н-катионитов.
Обратный осмос.
Метод основан на прохождении воды через полупроницаемые мембраны (как правило, полиамидные). Вместе с солями жёсткости удаляется и большинство других солей. Эффективность очистки может достигать 99,9 %.
Различают нанофильтрацию (условный диаметр отверстий мембраны равен единицам нанометров) и пикофильтрацию (условный диаметр отверстий мембраны равен единицам пикометров).
В качестве недостатков данного метода следует отметить:
– необходимость предварительной подготовки воды, подаваемой на обратноосмотическую мембрану, поэтому нормой является использование системы, включающей модули предварительной механической и химической очистки воды;
– относительно высокие начальные затраты, и большую стоимость 1 л получаемой воды (дорогое оборудование, дорогие мембраны) в сравнении с водопроводной водой;
Электродиализ.
Основан на удалении из воды солей под действием электрического поля. Удаление ионов растворенных веществ происходит за счёт специальных мембран. Так же как и при использовании технологии обратного осмоса, происходит удаление и других солей, помимо ионов жёсткости.
Полностью очистить воду от солей жёсткости можно также дистилляцией.
ФИЛЬТРАЦИЯ
Использование фильтра позволяет значительно изменить качество воды. Однако, существует огромное разнообразие систем фильтрации (водоочистки). От простейших насадок на кран и фильтров-кувшинов до громоздких специализированных многоступенчатых систем с высокой производительностью. Не касаясь угольных (сорбционных) фильтров, можно сказать, что по конструкции основного фильтрующего модуля фильтры подразделяются на 4 типа:
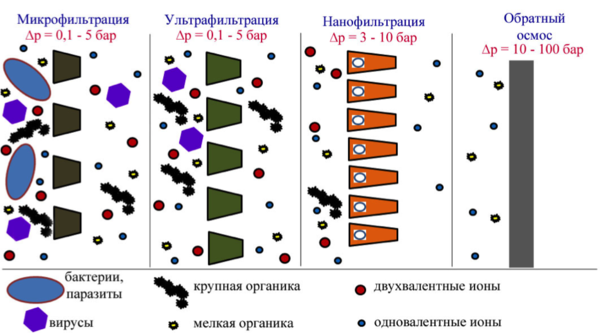
В комбинированных системах на разных ступенях могут быть использованы фильтры различного принципа действия. Наилучшего качества очистки можно достичь с помощью систем обратного осмоса. Явление осмоса лежит в основе обмена веществ всех живых организмов. Благодаря ему в каждую живую клетку поступают питательные вещества и, наоборот, выводятся шлаки. Явление осмоса наблюдается, когда два соляных раствора с разными концентрациями разделены полупроницаемой мембраной. Мембрана, работающая на основе обратного осмоса пропускает молекулы и ионы определённого размера, но служит барьером для веществ с молекулами большего размера. Таким образом, молекулы воды способны проникать через мембрану, а молекулы растворенных в воде солей – нет.
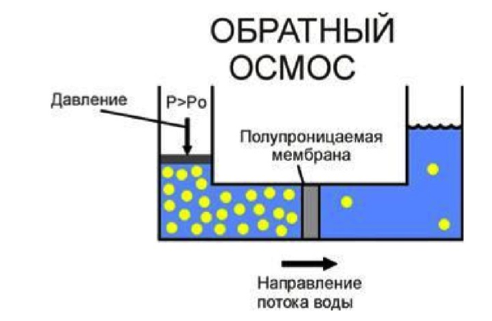
Если по разные стороны полупроницаемой мембраны находятся солесодержащие растворы с разной концентрацией то молекулы воды будут перемещаться через мембрану из слабо концентрированного раствора в более концентрированный, вызывая в последнем повышение уровня жидкости. Из-за явления осмоса процесс проникновения воды через мембрану наблюдается даже в том случае, когда оба раствора находятся под одинаковым внешним давлением.
Разница в высоте уровней двух растворов разной концентрации пропорциональна силе, под действием которой вода проходит через мембрану. Эта сила называется "осмотическим давлением". В случае, когда на раствор с большей концентрацией воздействует внешнее давление, превышающее осмотическое, молекулы воды начнут двигаться через полупроницаемую мембрану обратного осмоса в обратном направлении, то есть из более концентрированного раствора в менее концентрированный. Этот процесс называется "обратным осмосом". По этому принципу и работают все мембраны обратного осмоса.
В процессе обратного осмоса вода и растворенные в ней вещества разделяются на молекулярном уровне, при этом с одной стороны мембраны накапливается практически идеально чистая вода, а все загрязнения остаются по другую её сторону. Таким образом, обратный осмос обеспечивает гораздо более высокую степень очистки, чем большинство традиционных методов фильтрации, основанных на фильтрации механических частиц и адсорбции ряда веществ с помощью активированного угля.